Salut Louis-Marie

Je vais essayer d'être le plus claire possible, n'hésite pas si jamais ce n'est pas le cas !
Maîtresse donne un exemple avec un exercice, je vais me baser dessus pour te faire comprendre !
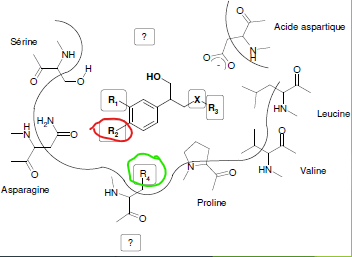
- mai1.png (20.73 Kio) Consulté 2179 fois

Prenons dans un premier temps
l'exemple de la liaison ionique. Une liaison ionique est en réalité une interaction électrique attractive entre cations et anions, tu devras te trouver en présence de 2 molécules de charges différentes, plus et moins.
Par exemple, en R2 et en R4, tu peux avoir une molécule de COO- et une molécule de NH3+, ainsi ton ligand et ton récepteur matcherons. En fait, tout est question d'équilibre.

Le jour de l'examen classant, Maitresse donnera des exemples plus simples. Elle vous mettra un site actif avec une partie de la molécule, puis elle vous demandera ensuite à quoi peuvent correspondre les groupements R1, R2, etc... Ce sera à toi en ayant connaissance des différents types d’interactions, uniquement faibles, de deviner quelles sont celles possibles et celles qui ne le sont pas !

En fait, pour bien répondre à cet exercice, il te faudra avoir bien
compris la partie sur les liaisons hydrogènes, les liaisons ioniques et les liaisons de Van der Walls !
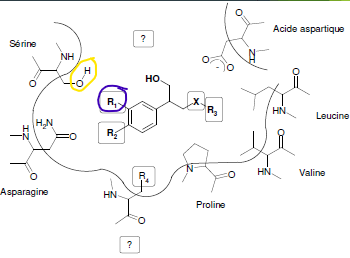
- maitresse 2.png (20.39 Kio) Consulté 2179 fois

Dans un second temps, prenons
l'exemple d'une liaison hydrogène ! La liaison implique forcément un atome d'hydrogène, je pense que jusque là je ne t'ai pas trop perdu !

De plus, elle se fait avec un atome électronégatif ayant des doublets non liants (oxygène, azote et fluor).

L'oxygène de la sérine peut former des liaisons hydrogènes, en effet, c'est un accepteur de liaisons H. Il faudra que sur le R1, on ait un atome avec un H.
 Attention
Attention, l'oxygène se lit à l'hydrogène d'un groupement donneur. Par exemple, le groupement R1 peut être un NH2.

Enfin, pour les 3 types de liaisons de Van der Walls, c'est le même système, une fois que tu as compris comment elles interagissent, tu sauras matcher à la perfection les différentes molécules ensembles !
 La spé pharma te souhaite un bon week end <3
La spé pharma te souhaite un bon week end <3 