Salut Briana ‼

Tout d’abord, il faut savoir qu'il y a plusieurs types d’hydratations sur les alcènes :
 Hydratation en milieu acide
Hydratation en milieu acide : avec H2SO4 dilué
 Hydroboration
Hydroboration : une hydratation en milieu basique avec BH3, H2O2/HO- et H2O

Il ne faut pas oublier que l’hydratation d’un alcène avec H2O uniquement est impossible. Car l’alcène est un centre riche en électrons donc il va réaliser des additions électrophiles. Or l’oxygène de l’eau possède 2 doublets non liants, donc H2O est un nucléophile.
Ainsi, l’hydratation doit se faire un milieu
acide ou
basique pour se réaliser.
Lors de la réaction d’hydratation en milieu acide, on utilise souvent comme acide :
H30+ (
H2O, H+) ou
H2SO4 dilué.
Cette réaction suit la
règle de Markovnikov qui dit que
l’électrophile se fixe sur le carbone le
moins substitué, tandis que le
nucléophile se fixe sur le
plus substitué.
La double liaison (nucléophile) attaque le H+ (électrophile). Selon la règle de Markovnikov, l’hydrogène va donc se fixer sur le carbone le moins substitué. On a généré un
carbocation. L’eau, présente dans le milieu, joue son rôle de nucléophile : 2 électrons libres de l’oxygène font une simple liaison avec le carbocation. L’oxygène ayant perdu 2 électrons devient +. On enlève un hydrogène et on obtient un alcool sur l’alcane.

Lors de l’
hydratation en milieu acide, on a la formation d’un
alcool qui va se situer sur le carbone de l’alcène initial le
plus substitué.
Enfin pour répondre à ta question, dans l’exemple que Maîtresse a donné (que je te remets en dessous), l’alcool formé est bien tertiaire.
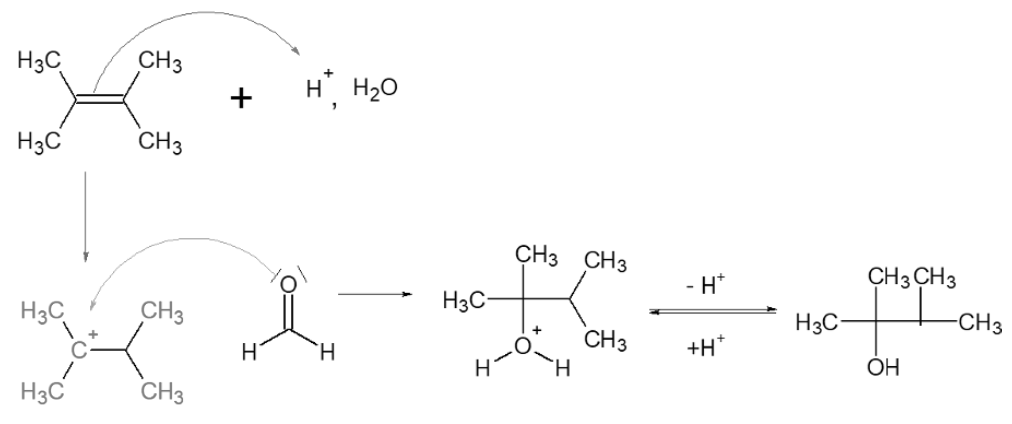
- Hydratation en milieu acide.png (54.14 Kio) Consulté 2443 fois

Pour rappel, un
alcool est dit
tertiaire lorsque le groupement hydroxyle est
porté par un carbone tertiaire, c’est-à-dire lié à trois atomes de carbone.
J'espère avoir été claire sinon n'hésite pas à le dire !
La team Chimie Orga est de tout cœur avec toi <33