Salut Youness !

Tout d’abord pour bien répondre à ta question je vais te faire un petit rappel sur une des propriétés des liaisons peptidiques : la
délocalisation des électrons.

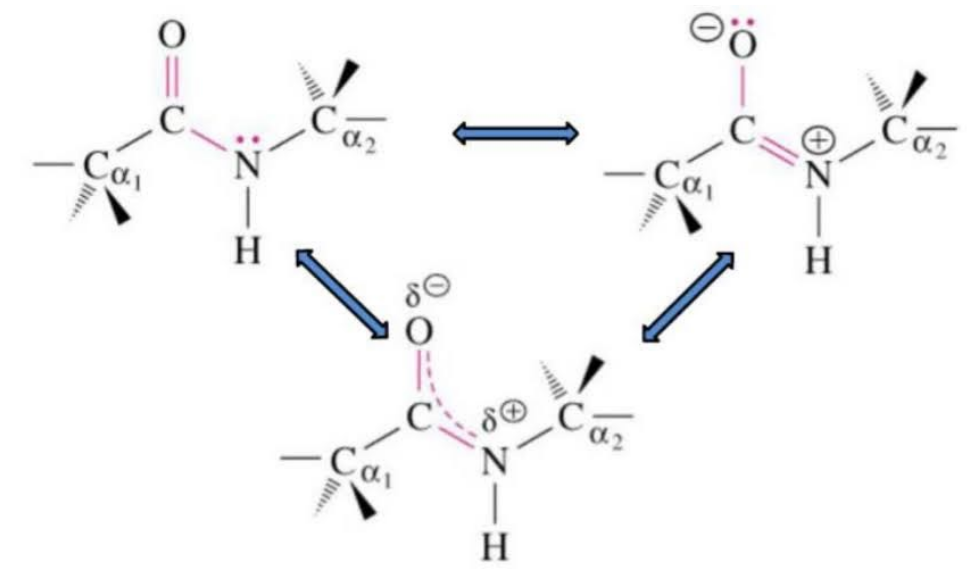
Dans la liaison peptidique, les électrons sont délocalisés sur les
3 atomes de la liaison : O, C, N. Cette délocalisation des électrons :
- place les 6 atomes qui entourent la liaison peptidique dans un même plan
- empêche la rotation de la molécule autour de la liaison C(1)-N.
- Capture d'écran_20221123_150421.png (151.35 Kio) Consulté 507 fois
Ces deux points sont importants pour la suite. Pour que les 6 atomes soient dans un même plan, la liaison peptidique ne peut prendre que
2 conformations définit par
l’angle oméga ω fixe.
Les deux conformations de l’angle oméga sont :
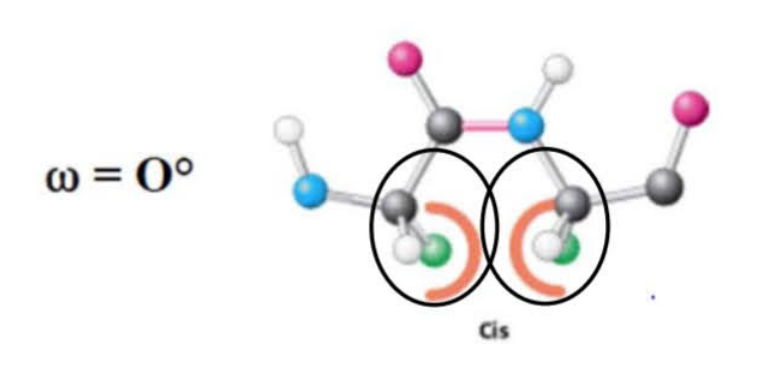
- ω=0° : la liaison peptidique est en conformation CIS
Cet angle est
défavorisé. Les carbones α et les chaînes latérales des deux acides aminés sont du
même côté. Ils sont donc très proches et se gênent. On parle d’un
encombrement stérique important.
- Capture d'écran_20221123_150435.png (113.19 Kio) Consulté 507 fois
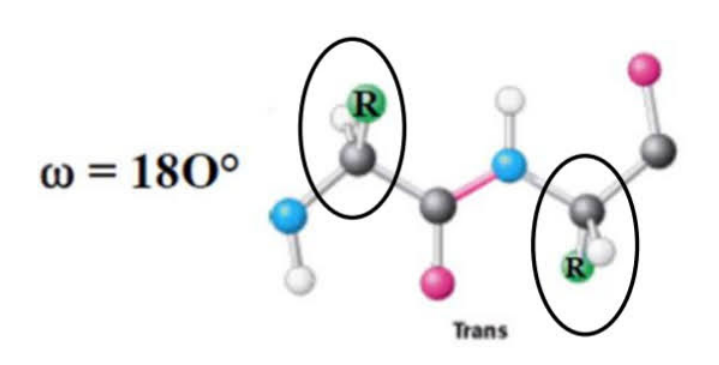
- ω=180° : la liaison peptidique est en conformation TRANS
Cet angle est
favorisé puisque les carbones α et les chaînes latérales sont
éloignés les uns des autres.
L’encombrement stérique est moindre.
- Capture d'écran_20221123_150448.png (106.79 Kio) Consulté 507 fois
Maintenant en effet, le professeur a précisé que pour des petits acides aminés tel que la glycine les deux configurations sont aussi possibles l’une que l’autre.
Mais pourquoi ? 
Puisque leurs
chaînes latérales sont très petites et donc
peu encombrantes. Prenons l’exemple d’une liaison peptidique de configuration CIS entre deux glycines (avec une chaînes latéral simple : H), les deux chaînes latérales ne se gêneraient pas même si elles sont du même côté (puisque petite chaîne latérale), l’encombrement stérique n'est pas très important.
J'espère avoir répondu à ta question, si c'est pas le cas n'hésite pas à reposer ta question. Si tu as d'autres questions l'équipe de Bioch' sera là aussi pour te répondre aussi

.
