Salut amel dy

Les réactions sur les organomagnésiens s'organisent toutes selon le même schéma réactionnel. Quand tu l'as compris, ce chapitre devient vraiment très simple

(en plus maitresse l'adore celui-ci, il faut bien le connaître) !
Un petit rappel sur les organomagnésiens :

Ils se présentent sous la forme
RMgX

Le X représente un
halogène (iode, chlore, brome). Les halogènes sont
très électronégatifs, ils ont donc un caractère
delta -.

Le Mg est un atome de
magnésium, qui est
très électropositif, il a donc un caractère
delta +.

Le groupement R correspond à une
chaine carbonée (maitresse insiste bien dessus). Comme il est lié à l'atome de magnésium, il porte un caractère
delta-.
Ainsi, quand on a une réaction avec des organomagnésiens, c'est
toujours le groupement R, chargé delta-, qui
va aller attaquer des groupements chargés delta+ (comme par exemple un carbonyle).

Toutes les réactions avec des organomagnésiens doivent
absolument être suivies par une hydrolyse (H2O) ou
hydrolyse acide (H3O+) pour pouvoir fonctionner !
Passons maintenant à la réaction que tu ne comprends pas ! Le mécanisme est le suivant :
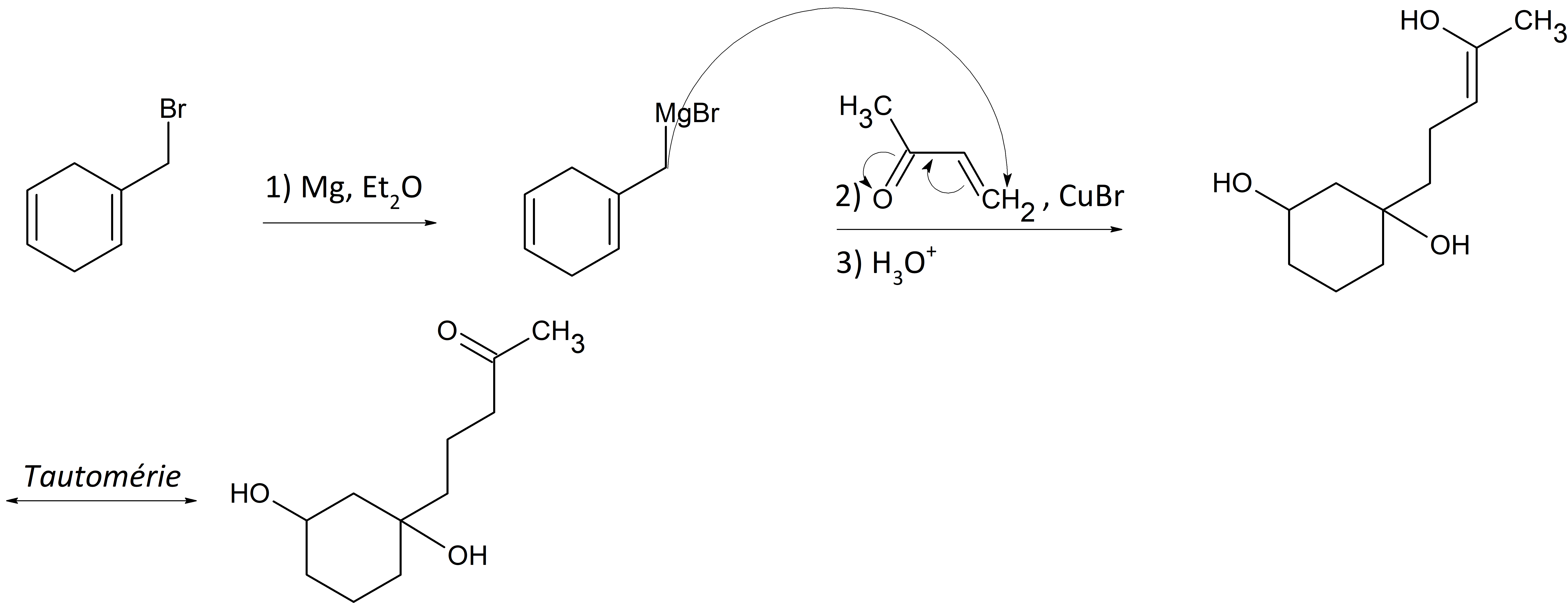
- organomagnésienss.png (164.93 Kio) Consulté 3091 fois
1) La première étape consiste en la
formation d'organomagnésien, où un halogénure d'alkyle de formule RX va réagir avec Mg, Et2O. On se retrouve avec une liaison formé entre l'atome de Brome et le magnésium. on a donc bien notre
RMgX.
2) La deuxième étape est une
addition d'un organomagnésien sur un carbonyle alpha, beta insaturé, en présence de sels de
cuivre CuBr, ce qui permet de réaliser une
addition 1.4 exclusivement !
3) La troisième étape est une
hydrolyse acide qui permet à l'addition 1.4 de se faire mais pas que ! Sur la molécule initiale, il y a 2 doubles liaisons. Or, tu sais depuis le chapitre des alcènes que lorsque l'on emploi H2SO4 dilué ou H3O+, cela correspond à une
hydratation des alcènes. Ainsi, selon la
règle de Markovnikov, la fixation des groupements hydroxyles (OH) sera sur le
carbone le plus substitué.
4) Enfin, il y a une étape de
tautomérie énol-cétone.

En résumé, dans cette réaction, l'hydrolyse acide (H3O+) permet d'exécuter l'addition des organomagnésiens sur le carbonyle alpha, beta insaturé et d'hydrater les deux doubles liaisons.
Le résultat est donc bon (même si la molécule a été pivoté d'une certaine façon)
J'espère que cette réaction est plus claire pour toi maintenant ! Si tu as bien compris le mécanisme de base des réactions sur les organomagnésiens, tout devrait se débloquer pour ce chapitre

! N'hésite pas à reposer une question si ça n'est toujours pas clair

Bonne chance pour tes révisions
