Salut !
Tout d'abord, j'espère que tu vas bien ! Je vais te faire un petit récapitulatif sur la réaction d'ozonolyse
avec et
sans réducteur en espérant t'éclairer
 Pour une réaction d'ozonolyse, tu auras toujours besoin des réactifs suivants :
Pour une réaction d'ozonolyse, tu auras toujours besoin des réactifs suivants :
 L'ozone (O3)
L'ozone (O3)
 Eau (H2O)
Eau (H2O)
Deux cas se présentent désormais : il est possible de réaliser une ozonolyse avec ou sans réducteur. Les réducteurs peuvent être le
diméthylsulfure (Me2S) ou le
triphénylphosphine (Ph3P).
 Ozonolyse sans réducteur
Ozonolyse sans réducteur
La double liaison de l'alcène est coupée et chaque carbone de la double liaison est
oxydé au maximum, c'est-à-dire jusqu'à la formation d'une
cétone ou d'un
acide carboxylique.
 Ozonolyse avec réducteur
Ozonolyse avec réducteur
La double liaison est également rompue et les deux carbones engagés dans la double liaison sont oxydés. Néanmoins, l'oxydation s'arrête au stade
d'aldéhyde ou de
cétone.
Donc tu n'auras jamais la formation d'acide carboxylique avec un milieu réducteur.
Mettons ça en pratique avec 2 exemples.
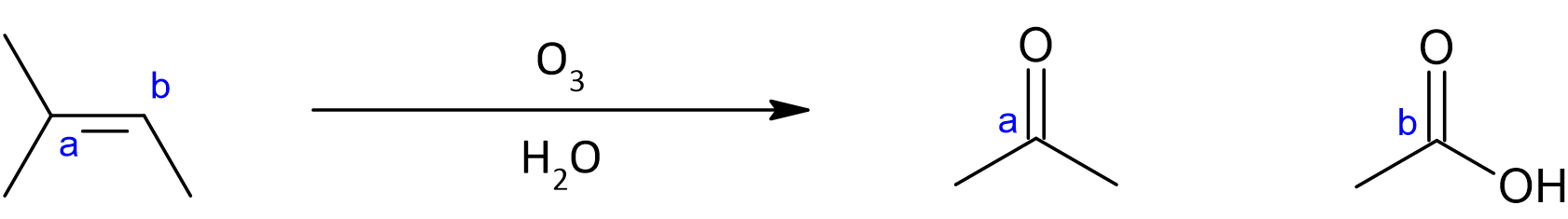
- Ozonolyse 1.png (15.58 Kio) Consulté 7373 fois
Tu peux voir ici qu'on réalise une ozonolyse sans réducteur donc l'oxydation va être maximale. Le carbone
a est oxydé jusqu'au stade de cétone car il est substitué par des groupements CH3 ce qui empêche la formation d'acide carboxylique (COOH). Le carbone
b est oxydé jusqu'au stade d'acide carboxylique car il est substitué par un seul CH3. Il reste un hydrogène disponible pour former le OH de l'acide carboxylique.
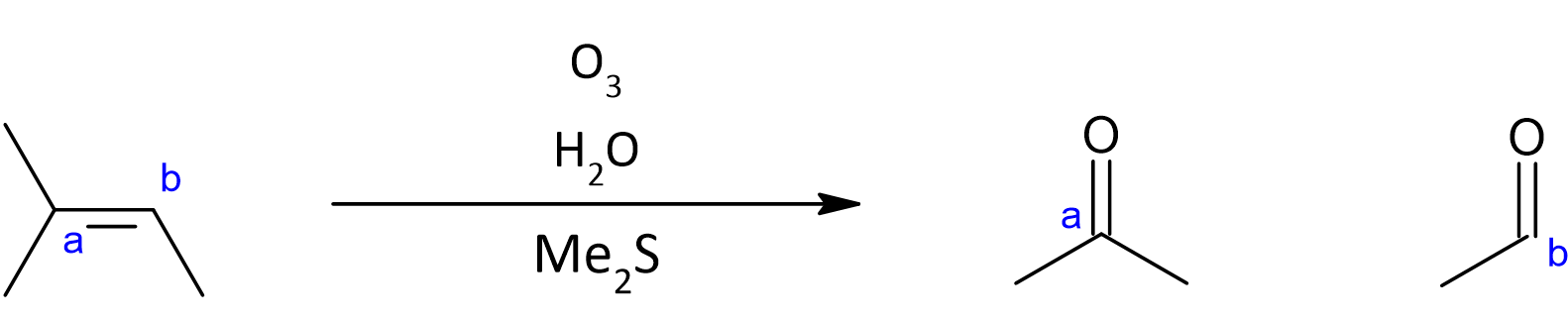
- Ozonolyse 2.png (17.51 Kio) Consulté 7373 fois
L'ozonolyse sans réducteur mène à la formation d'un carbonyle. Avec le carbone
a, ça donne encore une cétone. Avec le carbone
b, un aldéhyde est formé car le carbone n'est pas complètement substitué et le milieu réducteur empêche la formation de l'acide carboxylique.
J'espère que tout est plus clair pour toi !
Toute la team Chimie Orga te souhaite bon courage !!