Helloooo

Alors c’est vrai que les molécules à rallonge c’est pas toujours évident, donc je t’ai refait toute la réaction détaillée :
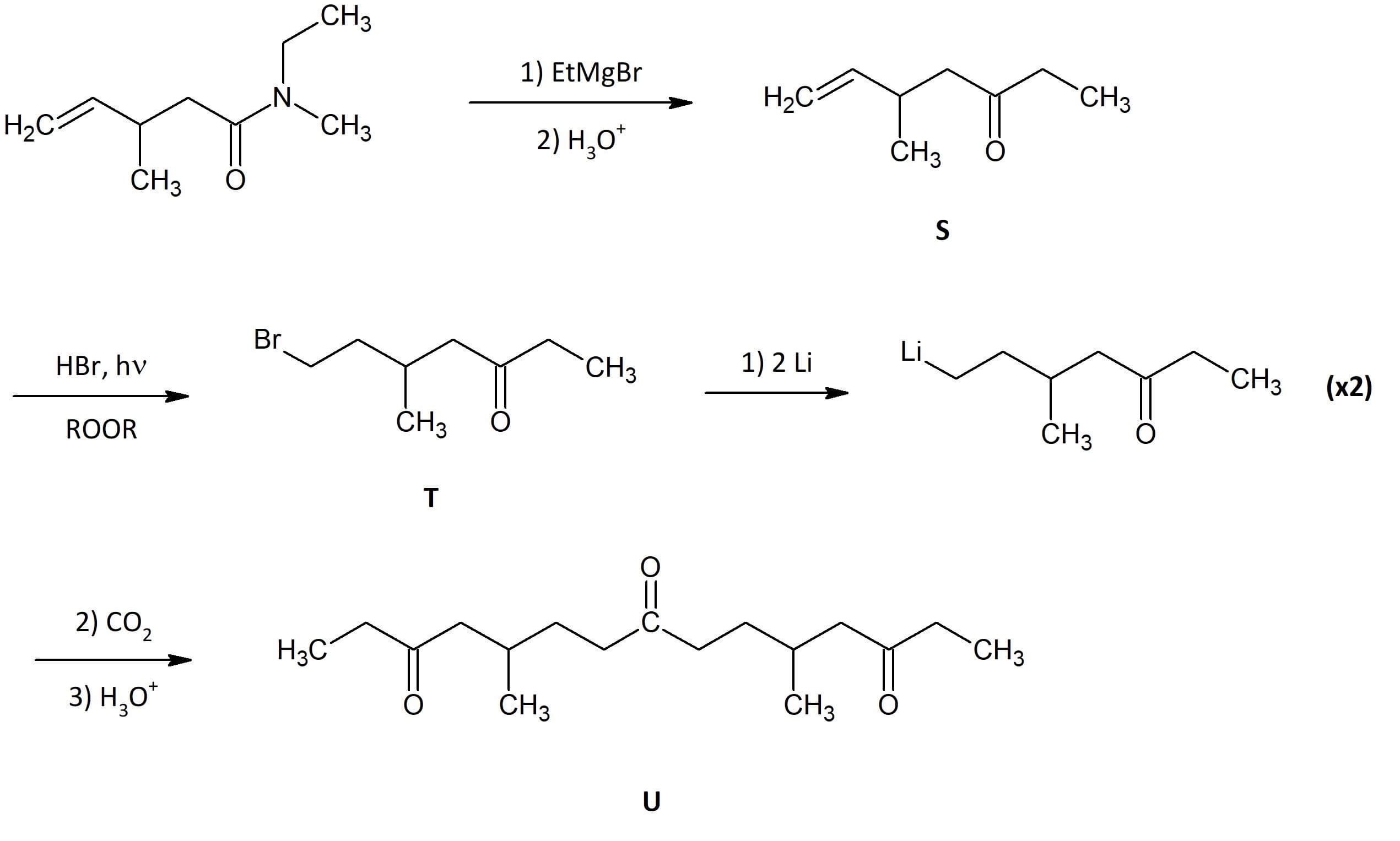
- F8B7D552-DC58-41DA-AB92-A60B745139C3.jpeg (202.15 Kio) Consulté 1438 fois
Explications :

En premier lieu, il s’agit d’une
formation de cétone à partir de la
réaction entre un amide et un organomagnésien, suivie d’une hydrolyse acide. Et sur notre molécule S, on a bien l’ajout de notre groupement éthyl (soit 2 carbones).

Ensuite, le passage de S à T est une
addition radicalaire, ainsi un atome de
Brome vient se fixer sur le
carbone le moins substitué (
effet Karash).

Ensuite je me suis permise de tout bien de détailler la dernière réaction pour bien que tu comprennes. On a dans un premier temps, la
formation d’un organolithien. Les organolithiens sont préparés à partir d’halogénures d’alkyles (ici, on en a bien un avec son atome de Brome) avec
2 moles de lithium.

Et enfin on a la
formation d’une cétone symétrique à partir de dioxyde de carbone, suivi d’une hydrolyse acide.
Et ne pas oublier : 2 MOLES DE RLI.

Alors oui, on remarque que dans ma molécule, il y a un carbone en plus que dans la molécule de ton sujet, mais cela est un erratum des années précédentes. Mais le principe reste le même

Mais si jamais tu retrouves ce QCM sur tHarmo, n’hésite pas à la signaler !!

Donc pour finir, j’espère que toutes ces explications sont claires, sinon n’hésite pas à nous relancer ou à venir nous voir en perm tut’ !

Bon dimanche à toi et toute la
team CO te souhaite bon courage
<33