Hello Youness !
J’espère que tu vas bien

No panic, on va reprendre ça ensemble !
Déjà, la formation des éthers peut se faire de
2 façons :
- Substitution nucléophile de type 2 (SN2)
- Addition sur double liaison
Et en effet, la formation des éthers par addition sur une double liaison, va se faire en présence :
- D’un
alcool ROH
- D’un
alcène (double liaison)
- D’un
catalyseur acide :
H+ ou H2SO4
Je te remets le détail de la réaction :
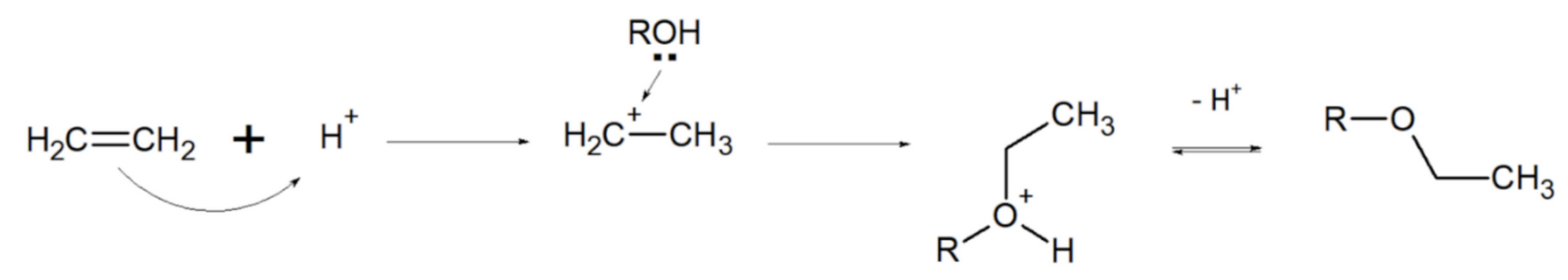
- 8811364F-0695-4395-AE1E-FE3D9803214D.jpeg (85.38 Kio) Consulté 1447 fois
Je m’explique :
1- Dans un premier temps, le
H+ étant un
électrophile, il va se faire attaquer par l’alcène (car je rappelle que les doubles liaisons sont riches en électron). Et cela va créer un carbocation.

On n’oublie pas la
règle de Markovnikov :
le carbocation doit être le plus stable possible, c’est à dire que ce sera le plus substitué.
2- Ensuite ton atome d’Oxygène, du groupement l’alcool, a des doublets non liants, ainsi il a des électrons en plus. Ces électrons vont aller
attaquer le carbocation et on a la formation d’une liaison entre le Carbone et l’Oxygène.
3- Et enfin, une relation de
tautomérie peut se faire pour conduire à notre éther.

C’est exactement le même principe sur la fiche qui vous a été distribuée. En effet, dans la molécule initiale, le groupement R est un éthyl- et on remarque que dans la molécule finale, on retrouve bien ce groupement éthyl- et également le groupement éthyl- qui correspond à celui de la double liaison.
Voilà ! J’espère avoir répondu à tes interrogations, sinon n’hésite pas à nous relancer !

Toute la
team CO t’envoie plein de courage pour cette dernière ligne droite !
<3