Hello Isma !
Ça va bien merci ! J’espère que tu vas également bien

On va reprendre ça ensemble, no panic !
Avant de commencer je te mets le détail de la réaction 1 :
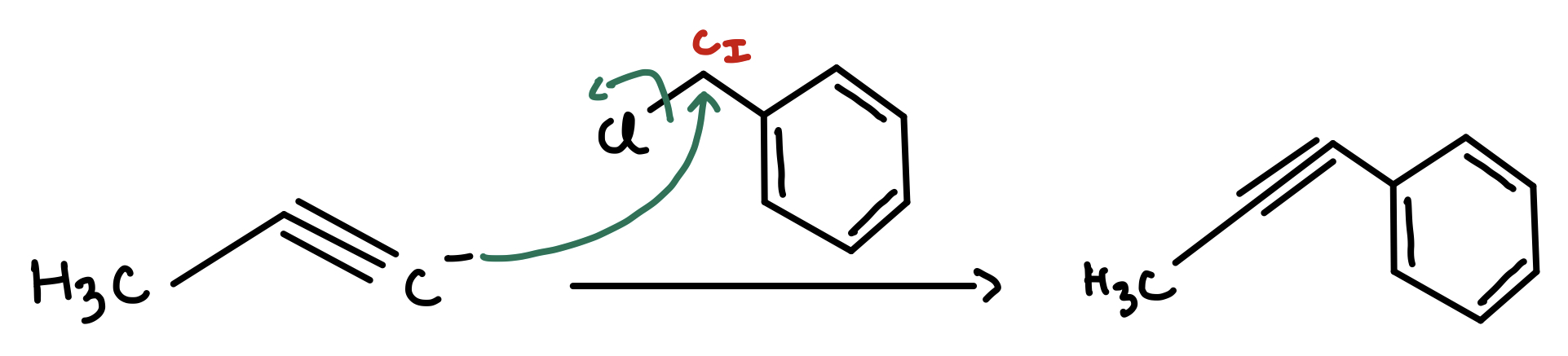
- DB0DA037-34DD-4D25-86F1-6BD21D19BDAC.jpeg (131.6 Kio) Consulté 1680 fois
Déjà on voit qui s’agit bien d’une réaction de substitution, car on vient remplacer l’halogène. Et comme il s’agit d’un halogénure d’alkyle primaire (en effet, le Chlore est relié à un carbone primaire). On parlera de
substitution nucléophile de type 2 (
SN2).

Je rappelle que les SN2 :
- Réagissent
très bien avec les halogénures d’alkyle
primaires
- Réagissent
bien avec les halogénures d’alkyle
secondaires
- Réagissent
pas du tout avec les halogénures d’alkyle
tertiaires
Et dans ce cas là
pas besoin d’ajouter de la chaleur ou quoi que ce soit, tu dois certainement confondre avec ce qui a été dit dans le chapitre sur les substitutions nucléophiles.
Dans le cas de la SN2, l’
ajout de base forte et l’
augmentation de température favorisent les réactions d’élimination de type 2 (
E2).
 Car je rappelle :
Car je rappelle : la SN2 est toujours accompagnée d’une réaction d’élimination. Mais la réaction SN2 est prépondérante sur la réaction E2, donc cela permettrait d’augmenter la proportion de réaction E2.
Voilà, voilà ! J’espère avoir répondu à tes interrogations et avoir été claire dans mes explications. Mais si cela n’est pas le cas, n’hésite pas à nous le faire savoir !

La
team CO t’envoie plein de courage pour cette dernière ligne droite !
<3