Page 1 sur 1
Benzènes Halogénation
Publié : 20 novembre 2020, 09:04
par Nitrazz
Bonjour à tous,
J'ai une question concernant l'halogénation des benzènes à laquelle je n'ai pas trouvé de réponse dans le forum :
L'acide de Lewis utilisé pour la réaction est-il spécifique du dihalogène utilisé ?
Je m'explique : doit-on obligatoirement utiliser du FeBr
3 avec le Br
2 et du AlCl
3 avec le Cl
2 ou bien on peut utiliser n'importe lequel des 2 acides de Lewis dans les 2 cas ?
Je ne souviens pas si Maîtresse l'a énoncé dans son cours donc si vous pouviez juste me préciser ce petit point, merci beaucoup !

Re: Benzènes Halogénation
Publié : 20 novembre 2020, 10:23
par Lauradius
Coucouuuuu Nitrazz

Tout d'abord j'espère que tu vas bien !

Tu as bien compris qu'il était nécessaire d'utiliser des acides de Lewis dans l'halogénation sur un benzène.
En effet, les halogènes ne sont pas suffisamment électrophiles et nécessitent donc un
accepteur de doublets d'électrons puissant pour les aider.

Pour répondre à ta question, il est préférable que
l'halogène présent dans ton acide de Lewis soit le même que celui utilisé dans ta réaction.

Ainsi :
-
Cl2 sera associé à
AlCL3
-
Br2 sera associé à
FeBr3
Pour t'expliquer, avec le
cas du brome par exemple :
Le brome possède 6 électrons libres. Il est associé à un acide de Lewis : FeBr3. Cela permet de créer un complexe : Br--Br+--FeBr3- (Le brome a perdu deux électrons et le fer en a gagné deux).
Ce complexe va permettre à la liaison de se polariser et de conférer un caractère
très électrophile à l'un des atomes de brome.
J'espère avoir bien répondu à ta question, sinon n'hésite pas !!

Toute la team te souhaite bon courage pour tes révisions, tiens bon c'est la dernière ligne droite !! <33
Re: Benzènes Halogénation
Publié : 20 novembre 2020, 10:36
par Nitrazz
Merci beaucoup pour ta réponse !
Je comprends totalement ton explication cependant quelque chose me "turlupine" : dans le qcm n°546 sur tHarmo, on fait réagir des dihalogènes avec les acides de Lewis "inverses" et cela semble fonctionner :
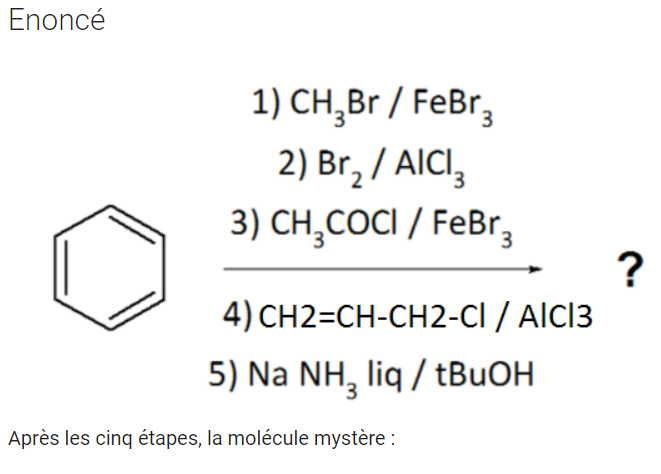
- Capturebenzenonce.PNG (84.37 Kio) Consulté 4733 fois
On trouve cette molécule au final :
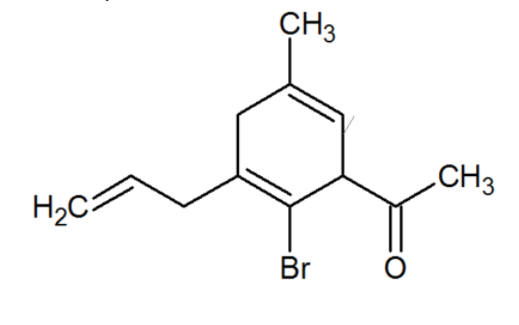
- Capturebenzmystere.PNG (23.13 Kio) Consulté 4733 fois
Aurais-tu de quoi me débloquer ?
Je dois sûrement faire une erreur de raisonnement mais je ne comprends pas pourquoi ça réagit dans ce cas...
Merci beaucoup !
Re: Benzènes Halogénation
Publié : 25 novembre 2020, 08:52
par Lauradius
Coucou Nitrazz,
Tout d'abord je m'excuse pour ma réponse si tardive,

Il est
préférable d'utiliser un acide de Lewis dont l'halogène correspond à celui utiliser dans ton acylation ou alkylation.
Cependant
l'inverse reste quand même possible.
Ce n'est donc pas une erreur mais un cas possible même si on utilise préférentiellement l'halogène correspondant

J'espère que c'est plus clair pour toi !

Courage pour tes révisions, donnes tout !! Pleins de love de la chimie orgaaaa <333
Re: Benzènes Halogénation
Publié : 25 novembre 2020, 12:45
par Nitrazz
Salut !
Merci beaucoup pour ces précisions !
Bonne journée et merci, on donne tout !

