Page 1 sur 1
ED n°1 P-C
Publié : 27 novembre 2023, 09:56
par 2207
Bonjour,
En re faisant le premier ED de physico chimie qu'on a eu, je ne comprends pas comment on déduit des calculs et de la réaction de dissociation du Ca(OH)2 que [OH-] = 2 * 10^-3 ?
Pourriez vous m'expliquer ?
Merci d'avance !
Re: ED n°1 P-C
Publié : 27 novembre 2023, 14:38
par Louise.m
Coucou, j'espère que tu vas bien !

D'après les données de l'exercice, on a la masse du Ca(OH)2 et la masse molaire du Ca. Ainsi on peut trouver le nombre de moles de Ca(OH)2 qui vaut :
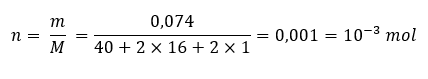
- Formule n.PNG (2.8 Kio) Consulté 4235 fois
De plus, grâce à un tableau d'avancement, on sait que la quantité de OH- à la fin de la réaction vaut 2n. Ainsi, on trouve 0,002
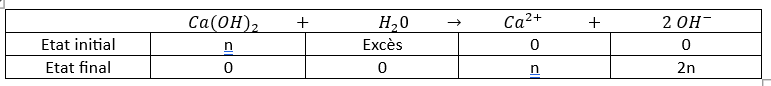
- ED 1 PC.PNG (4.43 Kio) Consulté 4235 fois
Ensuite, on peut calculer la concentration en OH - :
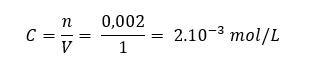
- Formule C.PNG (1.91 Kio) Consulté 4235 fois
Enfin, à l'aide de la formule du pH pour les bases fortes, on trouve que pH = 14 + log (C) = 14 + log (2.10^-3) = 11,3
J'espère que ça t'as aidé, l'équipe de physico-chimie te souhaite bon courage pour cette dernière ligne droite
